近日,国际化学领域顶尖期刊 Journal of the American Chemical Society (JACS) 在线发表了华中师范大学化学学院李俊容副教授与华中农业大学孙耀教授合作的最新研究成果。该研究针对肺癌循环肿瘤DNA(ctDNA)多重检测中单碱基变异(SNVs)识别极其困难且丰度极低的分析挑战,创新性地提出了一种中空异质结SERS纳米探针与微湍流增强电流体力(mt-EHD)界面的检测平台,为肺癌的精准液体活检与动态监测提供了新的技术方案。论文题目为《Molecularly Engineered SERS Platform with Microturbulence-Enhanced Electrohydrodynamics for Multiplexed Profiling of Lung Cancer ctDNA》。
肺癌ctDNA作为一种关键的液体活检标志物,在癌症早期诊断与预后监测中具有重要价值。然而,ctDNA在血液中含量极低,且常淹没在海量野生型DNA背景下,实现单碱基级别的精准识别难度极大。现有检测技术往往受限于探针的光谱重叠、信号增强通道单一以及固液界面传质效率低等瓶颈,难以满足临床多重实时分析的需求。团队创新性地从材料和界面出发,通过构建中空超支化Cu2O/CuO@Ag异质结纳米粒子,利用载流子寿命延长机制最大化电磁-化学双重增强效应。同时,团队在廉价铝箔上原位制备了纳米鹅卵石(nanopebble)结构的不对称微电极,利用该微形貌在电场下诱导产生强大的微湍流增强电流体力(mt-EHD),成功打破了界面流体的静态区,实现了靶标分子的主动富集和快速捕获。
该技术突破两个核心瓶颈:一是超灵敏信号放大机制,通过中空异质结构的能级调控抑制了电荷复合,实现了信号的显著提升;二是微湍流强化传质,利用纳米粗糙界面产生微湍流效应,显著缩短检测耗时的同时提升了信噪比。在131例真实的临床血浆样本中验证了6种关键ctDNA突变的同步定量,结合机器学习算法实现了肺癌的精准评估、预后分层及治疗监测。该项成果将分子设计、界面传质与临床诊断融为一体,颠覆了传统静态孵育的低效模式,为肺癌的精准诊疗提供了关键的技术支撑。
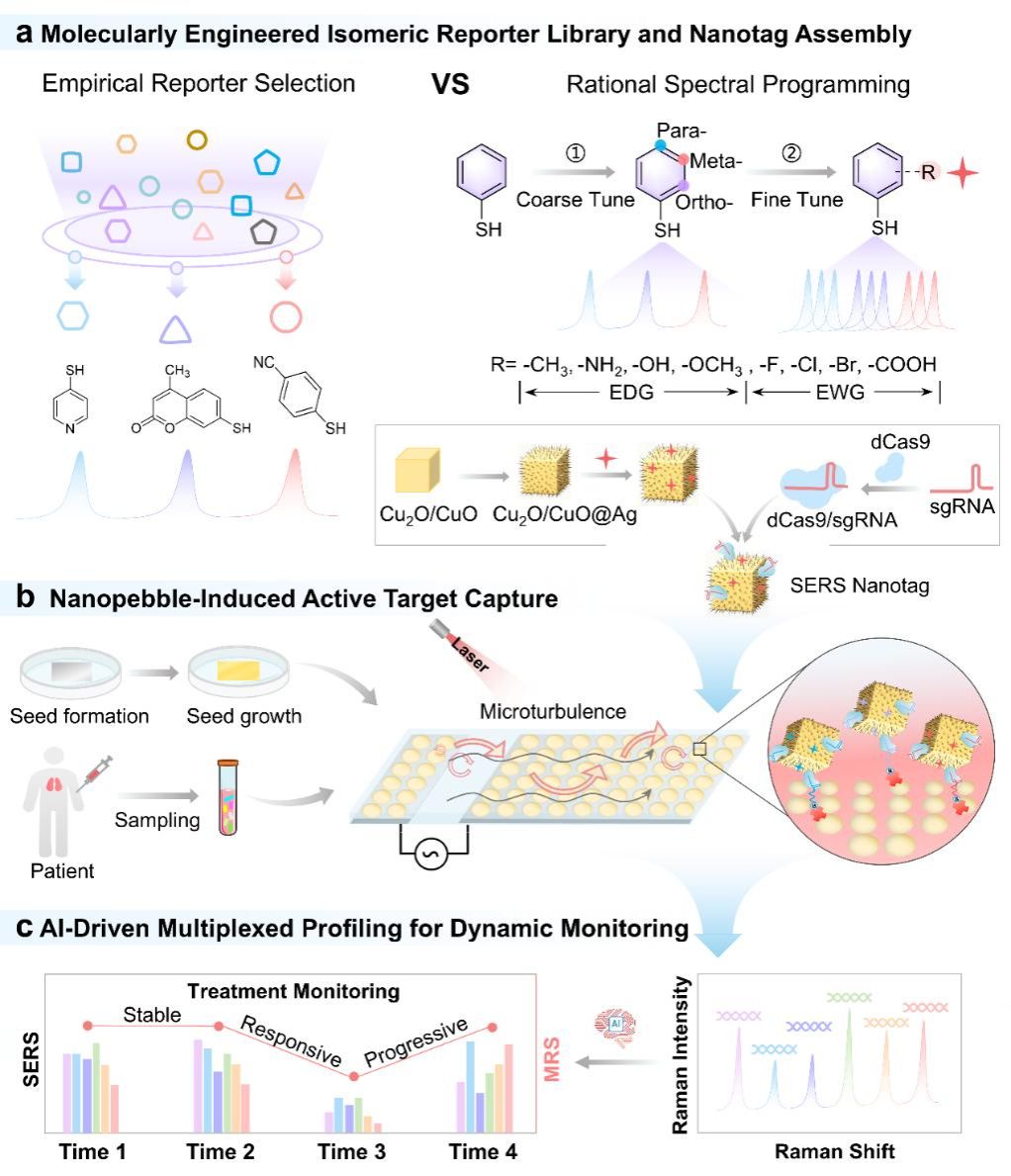
图1. 使用mt-EHD进行肺癌ctDNA多重分析的分子工程化SERS平台示意图。
李俊容副教授近年来聚焦基于表面增强拉曼光谱的生化分析与生物传感领域关键科学问题,建立了灵敏度高、精准度佳、通量数多的体外临床样品的病原体光学分析新平台,并取得了系统性的创新成果,多项研究发表于Nature Nanotechnology、Nature Communications、Advanced Science、Advanced Functional Materials、Analytical Chemistry等国际顶尖学术期刊。该项研究工作得到了国家自然科学基金面上项目、中国博士后科学基金、湖北省博士后创新人才支持计划、中央高校基本科研业务费等项目的支持。
文章链接:https://doi.org/10.1021/jacs.6c01526 (DOI: 10.1021/jacs.6c01526)